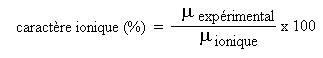Énoncé
La distance entre les deux atomes de la molécule de HCl est égale à 1.26 Å. Le moment dipolaire expérimental du gaz est 1.08 D. Calculer le caractère ionique de la liaison. S'agit-il d'une liaison covalente pure, covalente peu polaire, covalente très polaire ou ionique?
Réponse
Le caractère ionique d'une liaison chimique est estimé à partir de:
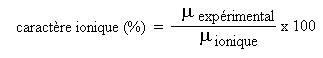
où:
μexperimental est le moment dipolaire réel (mesuré) de la liaison.
μionique est le moment dipolaire calculé en supposant la liaison complètement ionique:
μionique = (charge d'un électron) × (longueur de liaison)
Dans le cas de HCl:
μexperimental = 1.08 D = 1.08 × 3.33564×10-30 C.m
μionique = 1.6022×10-19 × 1.26×10-10 C.m
ce qui conduit à un caractère ionique de la liaison égal à 17.9%. La liaison dans HCl est donc covalente peu polaire.