
Composition typique des eaux
Eaux naturelles
| |
pC
pC=-log10C C = 10-pC
(C en moles/litre) |
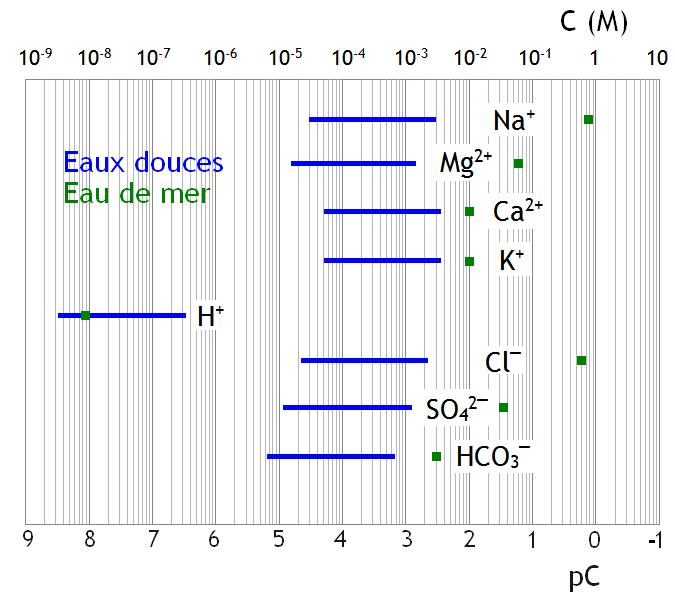
| Eaux douces | Eau de mer |
| Na+ | 3.6 ± 1.0 | 0.33 |
| Mg2+ | 3.8 ± 1.0 | 1.3 |
| Ca2+ | 3.4 ± 0.9 | 2.0 |
| K+ | 3.4 ± 0.9 | 2.0 |
| |
| H+ | 7.5 ± 1.0 | 8.1 |
| |
| Cl¯ | 3.7 ± 1.0 | 0.26 |
| SO42¯ | 3.9 ± 1.0 | 1.5 |
| HCO3¯ | 4.2 ± 1.0 | 2.6 |
Eaux en bouteille



Illustration
i.1
Quelle est, en mM, la molarité des ions Na+ dans l'eau de mer?
468 mM
i.2
À l'aide de l'information sur l'étiquette, calculez la molarité de chacune des espèces dissoutes dans l'eau en bouteille Naya. Vérifiez la validité de l'information à l'aide de l'équation d'électroneutralité de la solution.
Σ[+] = 4.98 mM; Σ[-] = 4.75 mM; analyse OK à 5% près

![]()



