![]()
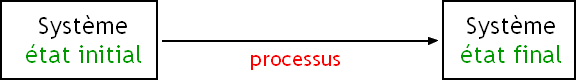
Eétat final - Eétat initial = ΔE;
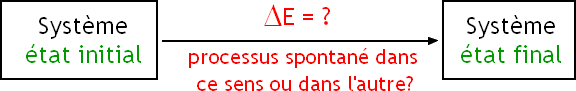

l'entropie d'un gaz est plus grande que celle d'un solide, par exemple
→ ΔG = ΔH - TΔS (à T constante)
→ ΔE = Q + W
→ q = ΔH (à P constante)
→ par exemple ΔH = CPΔT pour un chauffage à P constante, où CP est la capacité calorifique du système.
→ ΔS ≥ Q/T (à T constante)
→ ΔS ≥ ΔH/T (à T et P constantes)
→ ΔG ≤ 0 (à T et P constantes):
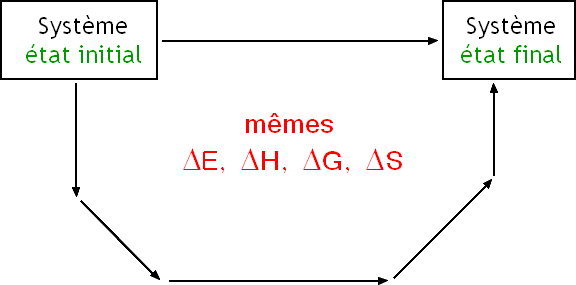
→ ΔE, ΔH, ΔS et ΔG qui accompagne un processus ne dépendent pas du chemin suivi;
→ on pourra calculer ΔE, ΔH, ΔS et ΔG pour n'importe quel processus complexe, en le décomposant en étapes simples