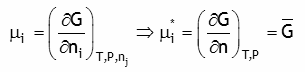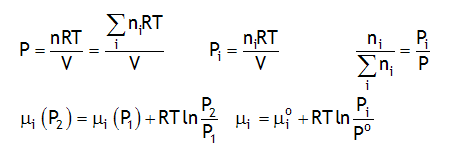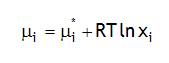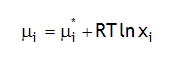On considère une solution aqueuse d'urée H
2NCONH
2 de molalité 0.1 m à 25ºC. En supposant que la solution est idéale:
- Lequel, de l'eau dans la solution et l'eau pure, possède le plus grand potentiel chimique?
- Calculez la différence de potentiel chimique de l'eau entre la solution et l'eau pure. Placez schématiquement les deux potentiels chimiques sur une même échelle verticale d'énergie, en y portant toutes les valeurs numériques connues.
- Effectuez les calculs et tracés correspondants pour l'urée. Peut-on regrouper les deux schémas sur une même échelle?
a) l'eau pure car x est toujours entre 0 et 1; b) μ = μ°-4.47 J.mol-1; c) μ = μ°-5.71 kJ.mol-1
![]()