
Volume molaire partiel - Définition et propriétés
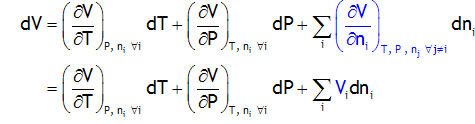
À température et pression constante:
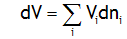
Exemple: Volume molaire partiel de l'eau dans les mélanges eau-éthanol
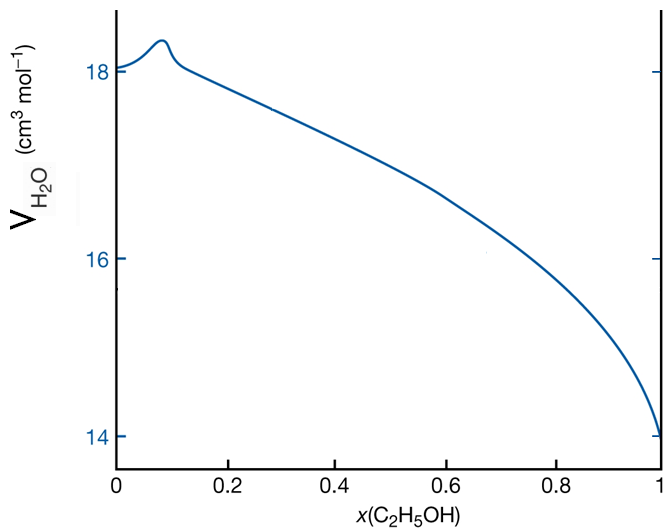
Vi est le volume occupé par une mole du constituant i dans le mélange à la composition considérée. Par exemple, le volume occupé par une mole d'eau dans une mélange équimolaire eau-éthanol est environ 17 cm3.
On peut calculer le volume de la solution à T et P constants à partir des volumes molaires partiels avec:
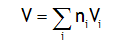

![]()
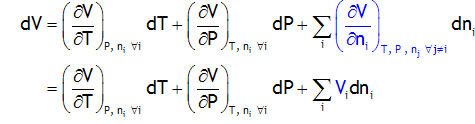
![]()

![]()