Énoncé
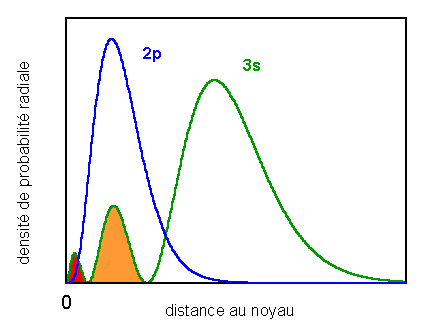
Tracer schématiquement la densité de probabilité radiale des orbitales 2p et 3s d'un atome polyélectronique. Que peut-on déduire de ces courbes en ce qui concerne la probabilité de présence des électrons de ces orbitales, en fonction de la distance au noyau?
Réponse
La figure nous montre que:
- l'électron dans une orbitale 3s
(
 )
possède une densité de probabilité maximum à une distance plus éloignée du noyau
que l'électron 2p
(
)
possède une densité de probabilité maximum à une distance plus éloignée du noyau
que l'électron 2p
( ).
Il est donc plus probable qu'un électron 3s se trouve à une distance plus grande du noyau qu'un
électron 2p.
).
Il est donc plus probable qu'un électron 3s se trouve à une distance plus grande du noyau qu'un
électron 2p.
-
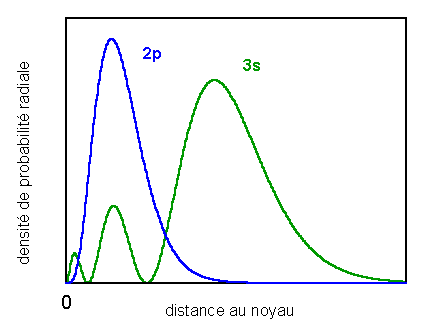
il existe malgré tout un probabilité non-négligeable de trouver l'électron 3s à environ la même
distance du noyau (
 )
ou même une distance plus courte du noyau
(
)
ou même une distance plus courte du noyau
( )
que l'électron 2p:
)
que l'électron 2p: