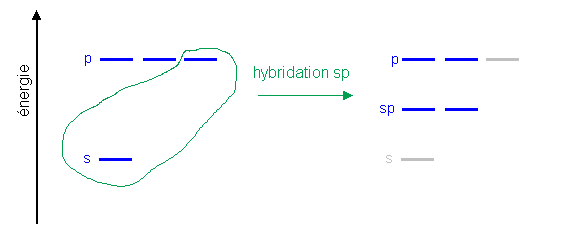
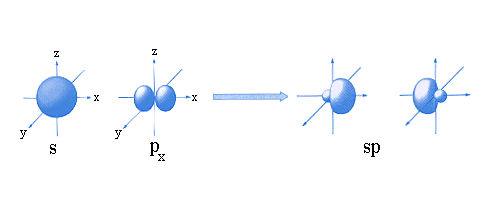
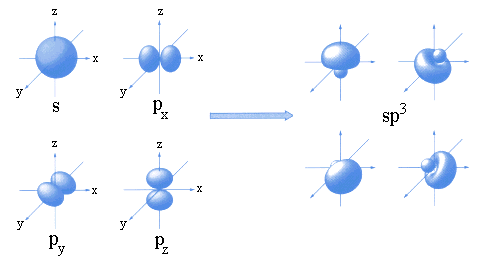
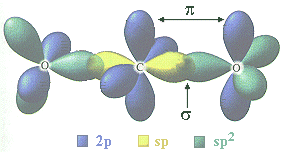
Les orbitales moléculaires font parfois intervenir des orbitales atomiques hybrides, telles que les orbitales atomiques hybrides sp:
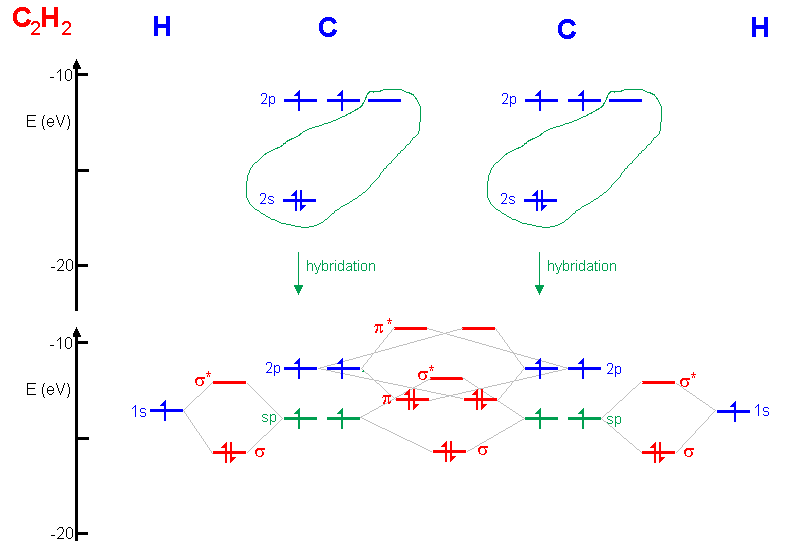
intervient par exemple dans la formation d'une orbitale moléculaire

dans la liaison C-H de l'éthylène C
2H
4, par combinaison linéaire avec une orbitale atomique
1s.
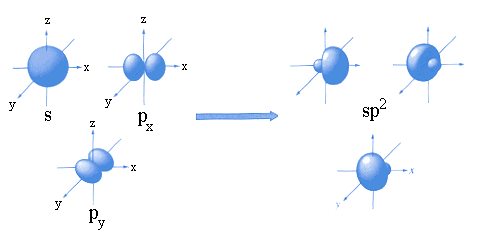
Les trois hybrides
sp2 sont dans le même plan, dans des directions orientées à 120° l'une de l'autre.