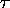 , des équilibres décrits à la première colonne.
, des équilibres décrits à la première colonne.

 (A= adénine, G=
guanine, C= cytosine et U= uracyl) se dimérise en formant une double
hélice
(A= adénine, G=
guanine, C= cytosine et U= uracyl) se dimérise en formant une double
hélice

- Une étude de cet équilibre par une méthode de relaxation
a été effectuée sur une solution
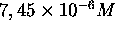 de
de 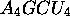 à pH 7: après une perturbation légère de l'
état d'équilibre initial produite par une élévation soudaine
de température jusqu'à T=305,5K, la relaxation du système vers
le nouvel état d'équilibre à cette nouvelle température est
suivie par spectrophotométrie. Le tableau suivant donne la variation
à pH 7: après une perturbation légère de l'
état d'équilibre initial produite par une élévation soudaine
de température jusqu'à T=305,5K, la relaxation du système vers
le nouvel état d'équilibre à cette nouvelle température est
suivie par spectrophotométrie. Le tableau suivant donne la variation 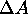 de l'absorbance de la solution à 265nm en fonction du temps
de l'absorbance de la solution à 265nm en fonction du temps
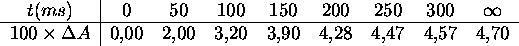
Sachant que
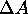 est proportionnelle à la concentration
instantanée du produit, déterminez le temps de relaxation
est proportionnelle à la concentration
instantanée du produit, déterminez le temps de relaxation 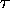 du
système dans les conditions de l'expérience.
du
système dans les conditions de l'expérience.
- On a répété l'expérience sous des conditions varié
es de concentration de
 , à
, à 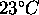 et à pH
7. Les résultats sont
et à pH
7. Les résultats sont
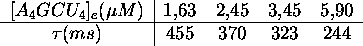
Déterminez les constantes
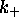 et
et 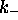 dans ces conditions de temp
érature et de pH.
dans ces conditions de temp
érature et de pH.

a été étudié par une méthode de relaxation. Les ré sultats suivants ont été obtenus dans des conditions STP

À partir de ces données, déterminez les constantes  et
et 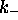 et la constante d'équilibre K de cette réaction.
et la constante d'équilibre K de cette réaction.

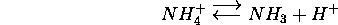
est caractérisée par 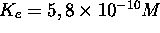 à
à  . On
connaît d'autre part la constante de vitesse
. On
connaît d'autre part la constante de vitesse  pour la protonation
de
pour la protonation
de  :
:
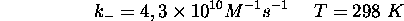
- Calculez la constante de vitesse
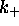 de l'ionisation de
de l'ionisation de 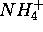 .
.
- Déterminez le temps de relaxation
 d'une solution 1M de
d'une solution 1M de 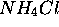 à pH 6 et
à pH 6 et 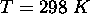

Le temps de demi-réaction pour la première réaction est de 15 jours, celui de la deuxième réaction est de 10 jours. Supposons qu'à un temps 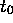 initial, on dispose d'un échantillon de
initial, on dispose d'un échantillon de 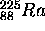 pur.
pur.
- Au bout de combien de temps l'actinium formé à partir de cet échantillon présentera-t-il une concentration maximale et quelle sera à cet instant l'abondance relative des deux éléments radio-actifs en présence? Peut-on supposer que
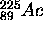 est dans un état stationaire?
est dans un état stationaire?
- Au bout de combien de temps l'abondance relative de ces deux éléments sera-t-elle, à
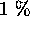 près, indépendante de t? (On dit alors que l'équilibre radioactif radioactif est atteint)
près, indépendante de t? (On dit alors que l'équilibre radioactif radioactif est atteint)