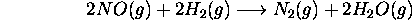
dans des conditions de concentrations initiales (exprimées sous la forme
de pressions partielles) variées, à 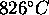 . Les ré
sultats sont
. Les ré
sultats sont

Énoncez la loi de vitesse de cette réaction.
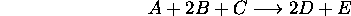
a été mesurée dans des conditions de concentrations initiales
variées. Les résultats sont (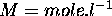 )
)

Déterminez l'ordre partiel de la réaction par rapport à A, B et C.
a été réalisée, à 298K, dans un ballon incompressible
contenant initialement du 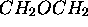 pur. On a obtenu les données
suivantes sur l'évolution de la pression totale
pur. On a obtenu les données
suivantes sur l'évolution de la pression totale 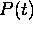

Déterminez, par une méthode de votre choix, l'ordre de cette ré action.
a été étudiée en mesurant le volume de  libér
é. On a obtenu les résultats suivants
libér
é. On a obtenu les résultats suivants
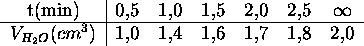
Sachant que  est proportionel à la concentration de
est proportionel à la concentration de 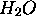 produit, montrez que cette réaction est du premier ordre.
produit, montrez que cette réaction est du premier ordre.
on a obtenu les données suivantes
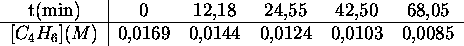
Montrez que cette réaction est du deuxième ordre.

a produit les données suivantes
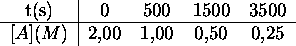
Déterminez, par une méthode de votre choix, la loi de vitesse de cette réaction.

on a trouvé que le graphe de  vs t est une droite de pente né
gative, et dont l'intercept à l'origine est
vs t est une droite de pente né
gative, et dont l'intercept à l'origine est 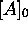 . Quelle est
l'ordre de cette réaction?
. Quelle est
l'ordre de cette réaction?


