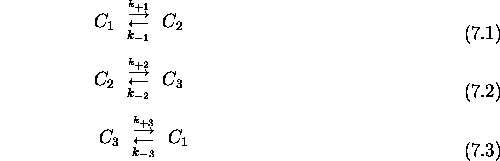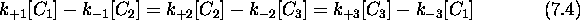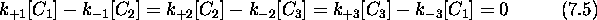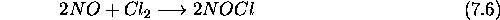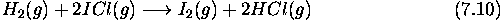Quand le système est à l'équilibre, non seulement a-t-on des
concentrations stationnaires des composés 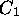 ,
, 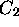 ,
, 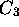 , ce qui
demande que les conditions
, ce qui
demande que les conditions
soient satisfaites, mais on doit forcément aussi avoir les trois équilibres (7.1), (7.2) et (7.3) atteintes séparément. En d'autres termes, on doit compléter eq.(7.4) comme suit
suit la loi de vitesse empirique suivante
ce qui suggère qu'elle est élémentaire. Si tel est le cas, on aurait une collision termoléculaire au cours de laquelle une liaison est rompue et deux liaisons sont formées simultanément. C'est un mécanisme peu probable. Le mécanisme suivant est plus plausible:
suit la loi de vitesse empirique suivante
Elle ne peut donc être élémentaire. Sa loi de vitesse est du second ordre tandis que sa molécularité serait de 3 si la réaction était élémentaire. En plus, dans ce cas, on aurait bris de 3 liaisons et formation de 3 nouvelles liaisons au cours d'une collision termoléculaire. C'est un évènement extrêmement improbable.