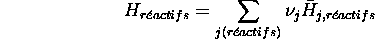Toute réaction chimique implique (absorbe ou dégage) de la chaleur:
Si q>0, la réaction absorbe de la chaleur et est dite\ endothermique. Dans le cas contraire, q<0, elle dégage de la chaleur et est dite exothermique. La plupart des réactions chimiques sont conduites à pression constante, et

où l'enthalpie de réaction 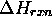 est
est
car ce qui est appelé ``produits'' constitue l'état final de la réaction, considérée un processus thermodynamique (le système est le ``système réactionnel''), et ce qui est appelé ``réactifs'', l'état initial du processus. Comme H est extensive, on a en outre
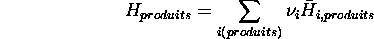
ou 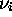 est le coefficient stoechiométrique de l'espèce
``produit'' i, et
est le coefficient stoechiométrique de l'espèce
``produit'' i, et 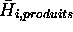 son enthalpie molaire. Il en est de
même pour les réactifs:
son enthalpie molaire. Il en est de
même pour les réactifs: