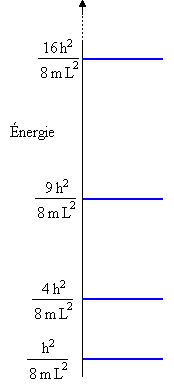Particules confinées dans une boite unidimensionnelle
Certaines molécules contiennent des électrons qui ne sont pas attachés à un noyau particulier, mais peuvent au contraire se déplacer assez librement dans une grande partie de la molécule. C'est le cas du β-carotène par exemple, dans lequel les électrons peuvent se déplacer linéairement sur toute la longueur de la molécule, ou encore de l'hème, un groupement porphyrique au coeur de l'hémoglobine, dans lequel les électrons peuvent se déplacer librement sur une surface carrée.
Pour une particule qui se déplace librement sur un segment de droite, de longueur L et tel que l'énergie potentielle Ep est nulle sur le segment et infiniment grande partout ailleurs (particule dans une boite), l'équation de Schröedinger se simplifie en:
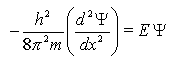
La résolution de cette équation différentielle conduit à une infinité de solutions. Cependant, les seules solutions acceptables sont celles qui vérifient:
- les valeurs aux bornes:
La particule se trouve sur le segment et non à l'extérieur, où Ep est +∞. La fonction d'onde, dont le carré mesure la densité de probabilité de présence de la particule, est par conséquent nulle à l'extérieur de la boite. Puis que Ψ est une fonction continue, on doit avoir
Ψ(0)=0 et Ψ(L)=0
- la condition de normalisation:
La probabilité de présence de la particule sur le segment entier, c'est-à-dire x entre 0 et L, est 100%:
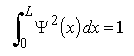
On obtient finalement, pour les fonctions d'ondes:
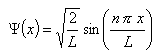
et pour l'énergie:
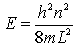
où le nombre quantique n est un entier strictement positif.
Énergies permises
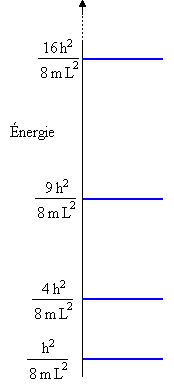
Illustration
i.1
Un électron est confiné dans une boite à une dimension de longueur 0.5 nm (à peu près la taille d'un atome). Calculez la différence d'énergie (exprimée en eV) entre les deux premiers états permis pour l'électron. Que devient le résultat pour une molécule de diazote N2 confiné sur un segment de 10 cm de long. Que peut-on en conclure?
4.51 eV; 2.21×10-21 eV
Cas d'une boite contenant plusieurs électrons
Lorsque le système contient plus d'une particule, une molécule par exemple qui contient plusieurs électrons, les solutions de l'équation de Schrödinger sont les mêmes (mêmes fonctions d'onde, mêmes énergies) mais il y a au plus deux électrons dont les propriétés ondulatoires sont décrites par une fonction d'onde donnée (principe d'exclusion de Pauli). On aura donc ici, à l'état fondamental au plus deux électrons de fonction d'onde n=1. Un troisième électron dans la boite serait décrit (même à l'état fondamental) par la fonction d'onde et l'énergie correspondant à n=2.
Illustration
i.2
Les polyènes conjugués linéaires sont des molécules constituées de liaisons carbone-carbone doubles et simples en alternance. Le butadiène, H
2C=CH-CH=CH
2, l'hexatriène, H
2C=CH-CH=CH-CH=CH
2, et l'octatétraène, H
2C=CH-CH=CH-CH=CH-CH=CH
2, en sont des exemples Ces molécules possèdent des électrons délocalisés, 2 pour chaque liaison C=C, dont les propriétés ondulatoires obéissent au modèle de particules dans une boite à une dimension. Sachant que chaque liaison carbone-carbone simple ou double contribue en moyenne 1.39 Å à la longueur de la boite:
- Calculer, pour chacune des trois molécules données en exemple, la longueur d'onde maximum du spectre d'absorption;
- déterminer le nombre de doubles liaisons dans le polyène de cette série qui possède un maximum d'absorption à une longueur d'onde égale à 843 nm.
a) butadiène: 114.7 nm; hexatriène: 227.5 nm; octatétraène: 346.8 nm; b) 8 doubles liaisons — Solution détaillée
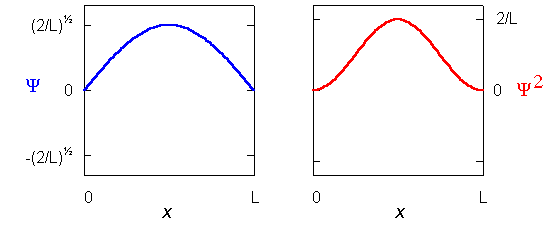
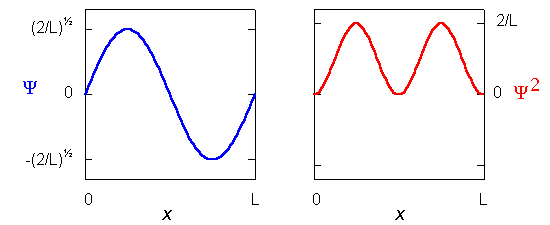
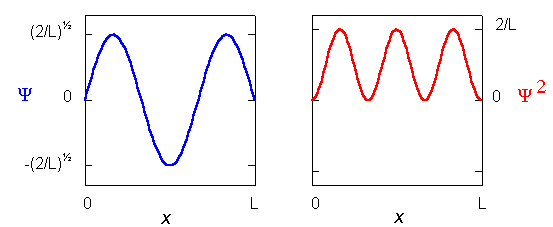
Fonctions d'onde et probabilité
La variation de la fonction d'onde Ψ et de la densité de probabilité Ψ2 en fonction de la position dans la boite dépend de n:
Illustration
i.3
Comment varie la probabilité de trouver une particule proche du milieu de la boite avec le nombre quantique n?
i.4
Montrez que les propriétés de la particule dans une boite sont conformes au principe d'indétermination de Heisenberg.
i.5
Montrez que la particule dans une boite obéit à la relation de de Broglie.
Solution

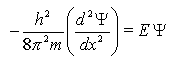
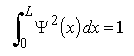
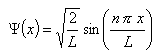
![]()