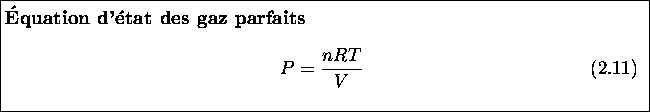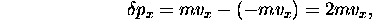
Un raisonnement similaire conduit à une première définition thermostatistique de la pression. Imaginons cette fois-ci que chaque molécule de vitesse
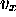 qui arrive sur
qui arrive sur 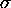 y subit une réflection élastique, c'est à dire
y subit une réflection élastique, c'est à dire 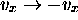 est la seule transformation que voit cette molécule sur la surface. Elle lui transfère alors (au cours de cette collision élastique) une quantité de mouvement
est la seule transformation que voit cette molécule sur la surface. Elle lui transfère alors (au cours de cette collision élastique) une quantité de mouvement
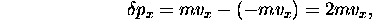
figure 2.2.
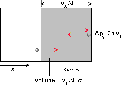
Figure: Collisions des molécules d'un gaz parfait sur une surface d'aire 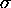 . Une molécule, animée de la vitesse
. Une molécule, animée de la vitesse 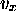 , échange avec la surface une quantité de mouvement
, échange avec la surface une quantité de mouvement
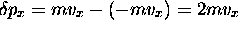 .
.
Comme il y aurait 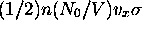 rencontres de ce type par seconde, la quantité de mouvement totale transférée du gaz à la surface par seconde, en d'autres termes, la force exercée par le gaz sur la surface, serait
rencontres de ce type par seconde, la quantité de mouvement totale transférée du gaz à la surface par seconde, en d'autres termes, la force exercée par le gaz sur la surface, serait
Moyennant sur la distribution des vitesses de Maxwell-Boltzmann en utilisant eq.(2.6), on obtient
ou encore